大阪大学大学院医学系研究科
呼吸器・免疫内科学
Department of Respiratory Medicine and Clinical Immunology, Graduate School of Medicine, The University of Osaka
副腎皮質ホルモン(ステロイド)は、全身性エリテマトーデス (SLE)、多発筋炎/皮膚筋炎 (PM/DM)、混合性結合組織病 (MCTD)など多くの免疫疾患の治療の柱と位置づけられています。吸入薬としての使用は、喘息の基本的治療であり、発作の頻度、重症度を減らし喘息の治療管理が容易になりました。副腎皮質ホルモンは、免疫アレルギー内科領域のみならず、臨床の各科においても重要な薬のひとつとなっています。
副腎皮質ホルモンの構造、生物学的活性の発見に関して1950年ノーベル生理学医学賞がEdward Calvin Kendall (Mayo Clinic, USA)、Tadeus Reichstein (Basel Univ., Switzerland)、Philip Showalter Hench (Mayo Clinic, USA)に授与されています。KendallとReichsteinが米国と欧州にて、競うように副腎皮質ホルモンの精製、構造決定を行いました。Kendallと同じMayo Clinicで働くリウマチ医であったHenchが、関節リウマチの患者さんに投与したところ、劇的な症状改善を示したことにより、副腎皮質ホルモンの持つ強い抗炎症作用が明らかとなりました。
その後、副腎皮質ホルモンは抗炎症作用のみならず多彩な副作用を持つことが明らかとなりました。疾患の重篤度と、治療目標を考えて投与量を決定し、副作用をモニターすると同時に、副作用対策の薬を併用しながら、副腎皮質ホルモンの抗炎症作用を治療に利用します。必要最小限の使用を心がけ、患者さんにも「作用と副作用」を説明し、理解して頂くことが大切と思います。
ステロイドは、細胞膜を通過後、細胞質のグルココルチコイドレセプター(GR: glucocorticoid receptor、ほぼすべての細胞に存在する)に結合する。ステロイドの結合したGRは、核内へ移行し、標的遺伝子の発現を転写因子レベルで調節すると考えられている。転写因子NF-κBやAP-1などと相互作用することが報告されている。この結果として、炎症に関与するサイトカインなどが負に制御され、免疫抑制作用が発揮される。
| 作用時間、種類 | 用量/日 | 抗炎症 作用 |
電解質 作用 |
生物学的 半減期 (hr) |
|
|---|---|---|---|---|---|
| 短 | コルチゾン cortisone |
12.5~ 150mg |
0.7 | 1 | 8-12 |
| ヒドロコルチゾン hydrocortisone |
10~ 120mg |
1 | 1.6 | 8-12 | |
| 中 | プレドニゾロン prednisolone |
2.5~ 60mg |
4 | 0.8 | 18-36 |
| メチルプレドニゾロン methylprednisolone |
2~ 48mg |
5 | 0 | 18-36 | |
| 長 | デキサメサゾン dexamethasone |
0.25~ 8mg |
25 | 0 | 36-54 |
| ベタメタゾン betamethasone |
0.25~ 8mg |
25 | 0 | 36-54 | |
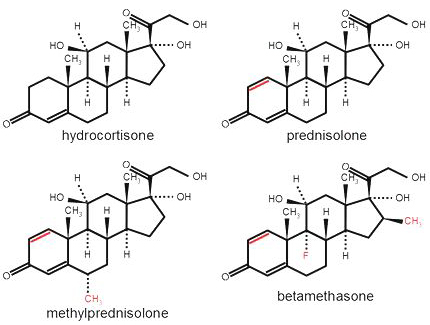
コルチゾン(商品名、コートン25mg錠)、ヒドロコルチゾン(コートリル10mg)、プレドニゾロン(プレドニン5mg錠、プレドニゾロン1mg錠・5mg錠)、メチルプレドニゾロン(メドロール4mg錠)、デキサメサゾン(デカドロン0.5mg錠)、ベタメタゾン(リンデロン0.5mg錠)
| 副作用 | 対策 |
|---|---|
| 血圧上昇 | 高血圧に対する対応(減塩、降圧薬、利尿薬など) |
| 浮腫 | 体液管理(利尿薬の調整、過剰な水分を制限)、減塩 |
| 耐糖能障害 | 肥満の是正、糖尿病に対する対応(食事療法、投薬、インスリン使用など) |
| 脂質代謝異常 | 高脂血症に対する対応(食事療法、肥満の是正、投薬) |
| 骨粗鬆症 | カルシウム摂取、適度な日光暴露と運動、骨粗鬆症に対する内服(ビスホスホネート製剤、ビタミンD・Kなど) |
| 骨頭無菌性壊死 | 局所の安静(荷重負荷を避ける、歩行しない、松葉杖など) |
| 易感染性 | 栄養状態の維持、感染予防行動(手洗い、うがい、マスクなど)、予防内服(抗結核薬、ST合剤など) |
| 消化性潰瘍 | 制酸薬の投与、ピロリ菌の除菌、NSAIDS(鎮痛薬)使用の抑制 |
| 筋力低下 | ステロイド減量、リハビリや適度な運動 |
| ムーンフェイス | ステロイド減量 |
| 中心性肥満 | ステロイド減量 |
| 精神症状 | ステロイド減量、精神科・神経科的な管理(安定剤など) |
| 不眠 | 睡眠導入剤の使用 |
| ざ瘡(にきび)、皮膚線条 | |
| 白内障、緑内障 | 眼科的なコントロール |
| 白血球増多 | |
| 低カリウム血症 | カリウム含有量の多い食品の摂取(野菜、果実など)、カリウム製剤内服 |
| 副腎不全 | 減量のスピードを緩める、ステロイドの補充 |
少量のグルココルチコイドは関節リウマチや他のリウマチ性疾患に有用であるが、その副作用により患者や医師の間で賛否両論がある。許容できる副作用の範囲での長期グルココルチコイド使用の条件に関するEULARタスクフォースからのコンセンサスが提案されている。
(1)プレドニゾン換算5mg/日以下で心血管リスクが高くなければ副作用は許容される。
(2)10mgを越える場合はステロイド抵抗性でなければリスクが利益を上回る。
(3)5mgを越え10mg以下の量では副作用リスクの評価には患者側の要素を考慮する必要がある。
ステロイドがSLEに対してしばしば著効し、喜んでいても、その後に大腿骨頭壊死を併発して無念な思いをすることがある。
大腿骨頭壊死のリスク因子として大腿骨頸部骨折などの外傷以外にも、ステロイド投与、SLE、アルコール摂取、高脂血症、高尿酸血症、喫煙、妊娠、腎不全、過凝固など多くの要因が関与することが知られている。大腿骨頭壊死は単純レントゲンで明瞭でない場合でもMRI撮影では感度良く診断される。ステロイドによる骨壊死の機構として、高脂血症による微小塞栓、骨髄内脂肪細胞の増大による血流阻害、静脈内皮障害から静脈鬱帯をきたし骨内圧を上昇させ骨壊死に至るなどの仮説が提唱されている。臨床でのステロイド使用と骨壊死の関係に関しては多くの報告があるが、残念ながら症例報告や後ろ向き研究報告が主でコントロールを置いた質の高い臨床試験は少なものの、ステロイド総投与量やステロイド投与期間よりも初期投与量が多い場合に骨壊死をおこしやすく、またムーンフェイスなどのクッシング様外見を呈すると骨壊死をおこしやすいという報告がある。画像診断手段による違いもあるがSLE患者では3~30%の頻度で骨壊死が生じるとされ、治療開始後1年目にMRIで異常がなければ以後の骨壊死のリスクは低いとされるが、年余を経て発症することもある。
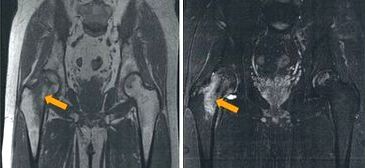 左:T1強調像、右:脂肪抑制T2強調像
左:T1強調像、右:脂肪抑制T2強調像
動物実験ではウサギへメチルプレドニゾロン(20mg/kg)を投与した場合、4週後に43%に骨壊死が発生し、壊死領域動脈に血栓を認め、6週後では血管再生像を認めている。ステロイドの種類では、メチルプレドニゾロンはプレドニゾロンやトリアムシノロンより骨壊死頻度が高く、メチルプレドニゾロン投与後のコレステロール、トリグリセリド、遊離脂肪酸はより高値だった。ウサギにワーファリンと脂質降下剤を投与するとステロイド骨壊死頻度は低下している。
本邦の多施設試験で40mg/day以上のステロイド療法を行ったSLE患者60例では、30%で骨壊死を生じ、ワーファリン投与群(PT-INR=1.5-2.0、ステロイド開始と同時に3ヶ月以上投与)では有症状骨壊死の低下傾向があるものの有意差はついていない。しかし、骨壊死をきたしたSLE患者ではステロイドパルス療法を受けたものが多く(P<0.001)、ワーファリンのみではSLEへのステロイドパルスによる骨壊死予防は不十分ではないかと考えられている。高用量ステロイドにスタチン系を併用した米国の284例では、骨壊死は1%の低頻度との報告があるが、この報告には移植患者が多く含まれSLEやステロイドパルス症例の記載がない。
質の高い比較試験はないものの、実際の臨床現場では骨壊死を併発してしまうと歩行障害や整形外科的処置を必要としてしまうため、高用量ステロイド使用時にはワーファリンや脂質降下剤の併用を勧める論文もある。また、ステロイドパルス療法では凝固亢進のためヘパリン(10000単位/day)を併用することがある。