大阪大学大学院医学系研究科
呼吸器・免疫内科学
Department of Respiratory Medicine and Clinical Immunology, Graduate School of Medicine, The University of Osaka
喘息は「気道の慢性炎症を本態とし、変動性を持った気道狭窄や咳などの臨床症状で特徴付けられる疾患」である。気道上皮細胞とともに自然免疫と獲得免疫が慢性炎症に関与し、気道過敏性(冷たい空気や運動などの非特異的刺激に対する平滑筋の反応)、粘液過剰産生、気道壁リモデリング、気道狭窄を引き起こす。気道を舞台として様々な免疫細胞の活性化が基礎にあり、標的サイトカインを制御する治療も登場し、当院では呼吸器内科とともに免疫内科で診療することも多い。
本邦2004~2006年調査では成人の喘鳴の有症率10%、喘息有病率4.2%で増加の傾向にある。喘息患者は温暖地に多いが、年齢構成では2~3歳をピークに成長するにつれて低下し20歳頃に10分の1まで減少し最低となったあと、加齢とともに40歳以降まで成人発症特に中高年発症が増加していく。性別では14歳までは男性が多いが15歳以上は女性が多い。吸入ステロイド薬や長時間作用性の気管支拡張薬の普及による治療の進歩とガイドラインの普及により喘息死は減少し2017年には1,794人であった。92%が65歳以上で、85歳以上では女性の喘息死が多い。若年者の喘息死をゼロにするとともに高齢者の対策が重要である。
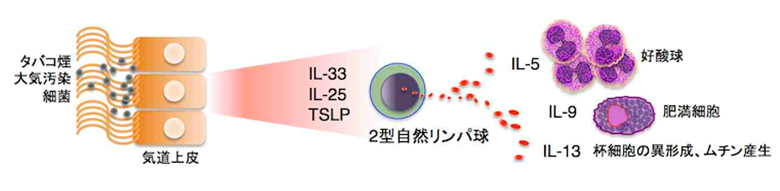
喫煙などの汚染物質や微生物、細菌の糖脂質などによる気道上皮細胞の障害から核内のalarminであるIL-33の放出、気道上皮細胞からIL-25やTSLP(thymic stromal lymphopoietin)が産生され、これらが抗原特異性を持たない2型自然リンパ球(group 2 innate lymphoid cells : ILC2)を刺激して増殖活性化しIL-5、IL-9、IL-13を産生する。IL-5は好酸球を増加させ、IL-9は肥満細胞の増殖や杯細胞の異形成に関与、IL-13は気道の杯細胞の異形成、ムチン産生や気道平滑筋の増生に関与する。
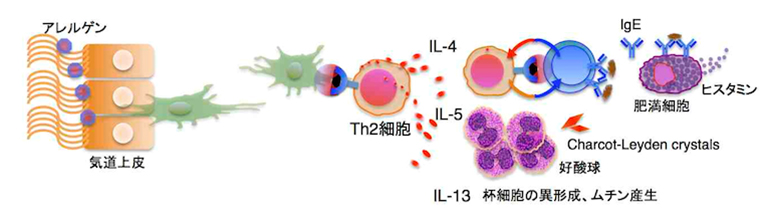
抗原特異的T細胞受容体を持つTh2細胞は樹状細胞からアレルゲン由来抗原の提示を受けて活性化され、IL-4、IL-5、IL-13を産生する。IL-4はB細胞の抗原特異的IgE産生をもたらす。IL-5は好酸球増加、IL-13はムチン産生を促す。B細胞によって産生されたIgEは肥満細胞の受容体に結合しヒスタミンを放出して血管透過性を亢進させる。Th2細胞の作用として総IgE濃度上昇や抗原特異的IgEが観察される。
こうした抗原非特異的ILC2と抗原特異的Th2の両者からなる炎症は2型炎症と呼ばれる。2型炎症によるIL-5作用として血中や喀痰中(2%以上)では好酸球増加を生じ、IL-4/IL-13の作用として呼気中一酸化窒素濃度(fractional exhaled nitric oxide : FeNO)や血中ペリオスチン(細胞外マトリックス蛋白質)が上昇する。好酸球集積現場では好酸球の細胞死で放出されるシャルコー・ライデン結晶(ガレクチン10蛋白質)によりさらに2型炎症が促進される。
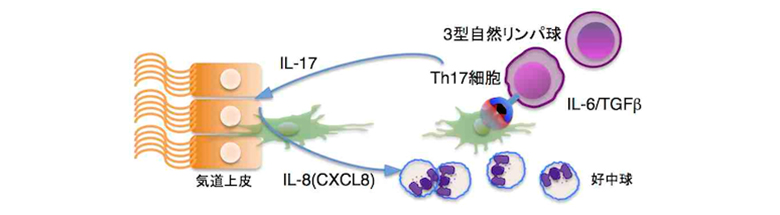
2型炎症や好酸球増加を伴わない、非2型炎症による喘息は好中球浸潤が目立ち、ILC3や、IL-6/TGFβにより分化したTh17細胞から産生されたIL-17が気道上皮に作用するとIL-8(CXCL8)が産生され、応じて好中球が遊走集積することが病態に関与している。喘息では2型炎症に非2型炎症が様々な程度で重なることもある。
喘鳴、息切れ、咳、胸部絞扼感などが変動を持って出現する。夜間や早朝に増悪する傾向がある。症状が感冒、運動、アレルゲン暴露、天候の変化、笑い、大気汚染、強い匂いなどで誘発される。症状が反復するエピソードの間に無症状の時期があることが確認できれば参考となる。追加の問診では病歴(症状の初発時期、過去の医療機関受診歴、投薬歴とその反応)、既往歴(アレルギー性鼻炎、薬剤や食物アレルギー)、生活歴(喫煙、常用薬剤、住環境、ペット飼育状況)、職歴と職場環境(勤務と症状との関連)、家族歴(アトピー素因、喘息)などを聞く。
症状の軽微なものや咳のみの場合は診断も難しく、気道可逆性試験や気道過敏性検査を行うことが正しい診断に大切である。呼気一酸化窒素濃度測定も有用である。
| 1 | 発作性の呼吸困難、喘鳴、胸苦しさ、咳の反復:これらはウイルス感染、運動、アレルゲン暴露、天候の変化、冷気や喫煙などの刺激で誘発されやすい。日内変動や季節性が見られ、夜間や早朝に悪化しやすい。 |
|---|---|
| 2 | 可逆性の気流制限:SABA吸入前後の呼吸機能改善。寛解期には可逆性を認めないこともある。治療や自然経過でFEV1が12%以上かつ200mL以上の変動、またはPEF値の20%以上の変動。気道リモデリングが生じた長期患者では可逆性に乏しいこともある。 |
| 3 | 気道過敏性の亢進:健常者では反応しない程度の弱い刺激によって気道収縮反応が起きる。 |
| 4 | 気道炎症の存在:喀痰好酸球3%以上、血中好酸球数220~320/μL、好酸球性気道炎症としてFeNOが35ppb以上。 |
| 5 | アトピー素因の存在:血清総IgE高値、種々のアレルゲンに対する特異的IgE抗体の存在。アレルギー疾患の既往歴・家族歴。 |
| 6 | 他疾患の除外:心不全や気管支結核、COPDなどとの鑑別が必要。喫煙者や高齢者では鑑別が難しいこともある。 |
1、2、3、6は診断に重要である。4が好酸球性の場合は診断的価値が高い。5は喘息の診断を支持する。
喘息との鑑別として以下の疾患を除外する。
上気道疾患(喉頭炎、喉頭蓋炎、vocal cord dysfunction)、中枢気道疾患(気管内の腫瘍、気道異物、気管軟化症、気管支結核、サルコイドーシス、再発性多発軟骨炎)、気管支~肺胞疾患(COPD、びまん性汎細気管支炎、肺線維症、過敏性肺炎)、循環器疾患(うっ血性心不全、肺血栓塞栓症)、薬剤(ACE阻害薬などによる咳)、その他(気胸、迷走神経刺激症状、過換気症候群、心因性咳嗽)。なおCOPDの特徴に喘息の特徴を併せもつ病態があり、ACO(asthma and COPD overlap)では吸入ステロイドの反応性が予測される。
変動性を持つ気道閉塞を検査するための呼吸機能検査と、気道慢性炎症を検査するFeNO測定や好酸球検査がある。
治療では、症状管理、リスク因子、合併症、副作用、患者満足度の評価を繰り返し、患者との同意の下で進めて行くことが基本である。実際には吸入ステロイド薬(ICS)を基本とし長時間作用性β2刺激剤(LABA)、長時間作用性抗コリン薬(LAMA)やロイコトリエン拮抗薬(LTRA)を適宜追加して行く。ICS量が多いほど重篤な急性増悪は少なくなるが、他の長期管理薬を追加するほうが治療成績は良い(エビデンスA)。ICSでは口腔咽頭カンジダ症、嗄声などの局所副作用があるので、吸入後のうがいを励行させる。しかし、ICSが結核を含めて呼吸器感染症のリスクをあげるという証拠はない。ICSとLABAの併用療法は相互に作用を増強させICSの減量が可能になるとともに喘息コントロールが良好になる(エビデンスA)。難治性喘息では抗IgE抗体、抗IL-5抗体、抗IL-5受容体α抗体、IL-4とIL-13を同時に阻害する抗IL-4受容体α抗体などが使用可能となっている。
| 症状 | 軽症間欠型相当 | 軽症持続型相当 | 中等症持続型相当 | 重症持続型相当 |
|---|---|---|---|---|
| 頻度 | 週1回未満 | 週1回以上、毎日ではない | 毎日 | 毎日 |
| 強度 | 軽度で短い | 月1回以上日常生活や睡眠が妨げられる | SABAが毎日必要。週1回以上日常生活や睡眠が妨げられる | 治療下でもしばしば増悪し、日常生活が制限される |
| 夜間症状 | 月に2回未満 | 月に2回以上 | 週1回以上 | しばしば |
| 目標治療 | 治療ステップ1 | 治療ステップ2 | 治療ステップ3 | 治療ステップ4 |
| 治療ステップ1 | 治療ステップ2 | 治療ステップ3 | 治療ステップ4 | ||
|---|---|---|---|---|---|
| 長 期 管 理 薬 |
基本 | 低用量ICS | 低~中用量ICS | 中~高用量ICS | 高用量ICS |
| 上記が使用出来ない場合下記のいずれかを併用 LTRA テオフィリン徐放製剤 |
上記で不十分な場合下記のいずれかを併用 LABA、LAMA、LTRA テオフィリン徐放製剤 |
下記の1剤か複数を併用 LABA、LAMA、LTRA テオフィリン徐放製剤 |
下記の複数を併用 LABA、LAMA、LTRA テオフィリン徐放製剤、抗体製剤 経口ステロイド、気管支熱形成術 |
||
| 追加 | LTRA以外の抗アレルギー薬 | ||||
| 発作治療 | SABA | SABA | SABA | SABA | |
ICS : 吸入ステロイド薬、
LABA : 長時間作用性β2刺激薬(配合剤でも使用可能)。吸入薬、貼付薬、経口薬がある。ICS/LABAの組み合わせはICS/テオフィリンンの組み合わせより優れる(エビデンスA)。
LAMA : 長時間作用性抗コリン薬(スピリーバ®)低~中用量のICSでの上乗せ効果はLABAと同等の効果がある(エビデンスA)。
LTRA : ロイコトリエン受容体拮抗薬(シングレア®、オノン®)。ICSへのLTRAの上乗せ効果はLABAと比較してやや劣る(エビデンスA)。
SABA : 短時間作用性吸入β2刺激薬。
抗体製剤 : 抗IgE抗体(オマリズマブ:ゾレア®体重や初回投与前のIgE値に応じた投与量となり2週から4週毎に皮下注)。抗IL-5抗体(メポリズマブ:ヌーカラ®末梢血好酸球数が150/μL以上の場合に有効性が高い エビデンスB。4週毎に皮下注)。抗IL-5受容体α抗体(ベンラリズマブ:ファセンラ®)。抗IL-4受容体α抗体(デュピルマブ:デュピクセント® 2018年ガイドラインには未収載)
LTRA以外の抗アレルギー薬:メディエーター遊離抑制薬(インタール®、リザベン®など)、ヒスタミンH1受容体拮抗薬(ザジテン®、アゼプチン®、ニポラジン®、アレジオン® などはアレルギー性鼻炎を有する場合に鼻炎の改善で喘息症状を改善させる可能性がある エビデンスB。)、トロンボキサンA2阻害薬(ベガ®、ブロニカ®など)、Th2サイトカイン阻害薬(アイピーディ®)
| ICS薬品名 | 吸入回数 | 低用量 | 中用量 | 高用量 |
|---|---|---|---|---|
| キュバール50,100エアゾール(大日本住友製薬) (ベクロメタゾンプロピオン酸エステル) |
1日2回 | 100-200μg / 日 | 400μg / 日 | 800μg / 日 |
| フルタイド50,100エアゾール(グラクソ・スミスクライン) (フルチカゾンプロピオン酸エステル) |
1日2回 | 100-200μg / 日 | 400μg / 日 | 800μg / 日 |
| フルタイド50,100,200ディスカス(グラクソ・スミスクライン) | 1日2回 | 100-200μg / 日 | 400μg / 日 | 800μg / 日 |
| オルベスコ50,100,200インヘラー(帝人ファーマ) (シクレソニド) |
1日1回 | 100-200μg / 日 | 400μg / 日 | 800μg / 日 |
| アズマネックスツイストヘラー100,200(MSD) (モメタゾンフランカルボン酸エステル) |
1日2回 | 100-200μg / 日 | 400μg / 日 | 800μg / 日 |
| パルミコート100,200タービュヘイラー(アストラゼネカ) (ブデソニド) |
1日2回 | 200-400μg / 日 | 800μg / 日 | 1,600μg / 日 |
| アニュイティ100,200エリプタ(グラクソ・スミスクライン) (フルチカゾンフランカルボン酸エステル) |
1日1回 | 100μg / 日 | 100 or 200μg / 日 | 200μg / 日 |
| ICS/LABA合剤薬品名 | 低用量 | 中用量 | 高用量 |
|---|---|---|---|
| アドエア100,250,500ディスカス(グラクソ・スミスクライン) (フルチカゾンプロピオン酸エステル/サロメテロールキシナホ酸塩) |
100を1吸入2回/日 200μg / 100μg |
250を1吸入2回/日 500μg / 100μg |
500を1吸入2回/日 1000μg / 100μg |
| アドエア50,125,250エアゾール(グラクソ・スミスクライン) (フルチカゾンプロピオン酸エステル/サロメテロールキシナホ酸塩) |
50を2吸入2回/日 200μg / 100μg |
125を2吸入2回/日 500μg / 100μg |
250を2吸入2回/日 1000μg / 100μg |
| シムビコートタービュヘイラー(アストラゼネカ) (ブデソニド/ホルモテロールフマル酸塩水和物) |
1吸入2回/日 320μg / 9μg |
2吸入2回/日 640μg / 18μg |
4吸入2回/日 1,280μg / 36μg |
| フルティフォーム50,125エアゾール(杏林製薬) (フルチカゾンプロピオン酸エステル/ホルモテロールフマル酸塩水和物) |
50を2吸入2回/日 200μg / 20μg |
125を2吸入2回/日 500μg / 20μg |
125を4吸入2回/日 1,000μg / 40μg |
| レルベア100,200エリプタ(グラクソ・スミスクライン) (フルチカゾンフランカルボン酸エステル/ビランテロールトリフェニル酢酸塩) |
100を1吸入1回/日 100μg / 25μg |
100または200 100,200μg / 25μg |
200を1吸入1日1回 200μg / 25μg |
吸入薬は正しく吸入されてはじめて効果を発揮するのでコントロール不良例に対しては吸入手技や吸入デバイスの見直しが必要となる。各吸入薬についての正しい吸入方法はWebサイト吸入療法サポートチャンネル「吸チャン」にて視聴できるので参照されたい。また、吸入時の口と喉の形について、「ホー吸入」を行うと吸入薬が舌表面につきにくく気管内に到達しやすい。
ICSのデバイスには主に2つある。粉末を吸入するドライパウダー定量吸入器(dry powder inhaler :DPI) では吸入に噴霧との同期は必要ないが、薬剤が肺内に到達するためにある程度の吸気流速が必要である。エアゾールを吸入する加圧噴霧式定量吸入器(pressurized metered-dose inhaler :pMDI)では吸入と噴霧の同期が難しいが、十分な吸気流量が得られにくい高齢者でも薬剤が肺内に到達しやすい。
| コントロール | 良好 (すべての項目が該当) |
不十分 (いずれかの項目が該当) |
不良 |
|---|---|---|---|
| 喘息症状(日中及び夜間) | なし | 週1回以上 | コントロール不十分の項目が3つ以上当てはまる |
| 発作治療薬の使用 | なし | 週1回以上 | |
| 運動を含む活動制限 | なし | あり | |
| 呼吸機能 (FEV1およびPEF) |
予測値あるいは 自己最良値の80%以上 |
予測値あるいは 自己最良値の80%未満 |
|
| PEFの日(週)内変動 | 20%未満 | 20%以上 | |
| 予定外受診、入院など | なし | 年に1回以上 | 月に1回以上 |
高用量の吸入ステロイドとLABAあるいは経口ステロイドによる治療にてもコントロール不十分な場合は、管理困難例(喘息そのものではなく、服薬遵守や吸入手技に問題があるなど他の要因が考えられる)なのか、重症難治例(他の要因を全て解決してもなおコントロールが不十分)なのかを鑑別する必要がある。オランダの報告では喘息患者のうちコントロール不十分が17.4%、そのうち服薬遵守と吸入手技が守られていたのは20.5%で、重症難治例は3.6%だった。コントロール不十分な場合では以下の要因を十分考慮する。
| 鑑別診断 |
・喘息と間違えやすい疾患が鑑別されているか 声帯機能不全、気管支結核や肺癌による気道狭窄、気管軟化症、気管支拡張症、COPD、心不全、誤嚥、ACE阻害薬など薬物による咳嗽など |
| 服薬アドヒアランス吸入手技 |
・吸入手技や服薬回数などの用法に誤りがないか ・長期管理の必要性が理解され、服薬アドヒアランスが良好か ・重症度やコントロール状態に応じた用量で薬剤が選択されているか |
| 合併症の管理 |
・喘息の重症化と関連する合併症の診断と治療が適切に行われているか 鼻炎、副鼻腔炎、COPD、胃食道逆流症、好酸球性多発血管炎性肉芽腫症、アレルギー性気管支肺真菌症、睡眠時無呼吸症候群、肥満、うつ病、不安症など。 |
| 増悪因子の確認と排除 |
・喘息を増悪させ得る薬剤が服薬されていないか NSAIDs、β遮断薬など ・職場、学校および家庭における増悪因子は適切に回避・除去されているか 喫煙、ダニ・真菌、ペットなどの感作アレルゲンなど |