大阪大学大学院医学系研究科
呼吸器・免疫内科学
Department of Respiratory Medicine and Clinical Immunology, Graduate School of Medicine, The University of Osaka
自己免疫疾患では気管支炎や細気管支炎などの気道病変以外に、間質、血管、胸膜などに多彩な肺病変をきたし、なかでも間質性肺疾患(ILD: interstitial lung disease)は予後を左右する。特に全身性強皮症や多発性筋炎/皮膚筋炎では主な死亡原因である。ILDは自己抗体によって特徴があり、抗MDA5抗体は急速進行性、抗Scl70抗体は慢性進行性、抗ARS抗体は再燃性などの経過をとりやすい。
診断では原疾患によるILD以外に感染症や薬剤性など他の要因による病態との鑑別が必要である。労作時呼吸困難や咳嗽などの症状から始まるが病初期では無症状も多く、吸期終末時での両側肺での捻髪音やベルクロラ音の聴診、胸部X線、胸部高分解能CT(HRCT)、呼吸機能検査、LDH、KL-6やSP-Dなどの血清マーカー、動脈血ガスなどで早期診断を行い、重症度と進行速度を判断し、予後予測に基づいて治療を選択する。必要に応じて気管支肺胞洗浄液解析や肺生検を考慮する。外来でのモニターは軽症では年一回、中等~重症では半年~年一回HRCTで進行性を評価する。
| UIP(usual interstitial pneumonia 通常型間質性肺炎) | |
|---|---|
| 肺胞隔壁の線維化による小葉辺縁性陰影。下肺野胸膜下優位で不均等に広がる不整線状影、網状影、軽微なすりガラス影、時に蜂巣肺も見られる。 | RAで多いがSScなどでも見られる。 |
| fNSIP(fibrotic nonspecific interstitial pneumonia 線維性非特異性間質性肺炎) | |
| 下肺野優位で比較的気管支に沿って広がる均等な網状影やすりガラス影。肺容積減少、牽引性の細気管支や気管支拡張を伴う。胸膜下のすりガラス影から繋がる、胸膜より内側の陰影が目立つ。 | SScで典型的なものが見られ、MCTDやSjSでも見られる。 |
| OP(organizing pneumonia 器質化肺炎) | |
| 肺胞腔内の器質化で、末梢胸膜下優位な非区域性浸潤影、すりガラス影、時に結節・塊状影を示す。進行すると器質化肺炎が構造境界に移りperilobular opacitiesやreversed halo signを呈することがある。RAでよく見られる。 | RAでよく見られる。 |
| FOP(fibrosing organizing pneumonia)/ NSIP with OP overlap | |
| 両側下肺野対称に容積減少を伴う気管支周囲の浸潤影。進行すると浸潤影は気管支血管や小葉隔壁などの構造境界に集中し索状影を呈する。NSIPとは異なりOP成分が多く急性~亜急性の経過を呈する。 | 筋炎、抗ARS抗体、抗MDA5抗体陽性で特徴的。 |
| DLH(diffuse lymphoid hyperplasia)/ LIP(lymphocytic interstitial pneumonia) | |
| リンパ球の間質への浸潤。肺胞隔壁への浸潤からすりガラス影や小葉中心性の淡い陰影、小葉間隔壁への浸潤から小葉間隔壁肥厚、気管支血管束への浸潤による気管支血管束肥厚や小葉中心性分岐粒状影が見られる。リンパ増殖性疾患の特徴として複数の嚢胞形成も見られる。 | SjSやRAなどで見られる。 |
| DAD(diffuse alveolar damage びまん性肺胞障害) | |
| 進行が早いのが特徴で、滲出期、器質化期、線維化期と線維化が進むほど容積減少と牽引性気管支拡張が目立つ。1ヶ月以内に転機がくる急性ループス肺炎などの超急性ではrandom分布、やや緩徐に進行する筋炎に見られる急性では下肺野対称性に分布する。 | SLEの稀な急性ループス肺炎、筋炎、UIPやfNSIPの急性増悪などで見られる。 |
| CBO(constrictive bronchiolitis obliterans 閉塞性細気管支炎) | |
| 細気管支炎パターンでは小葉中心性分岐粒状影が特徴だが、CBOのCT画像では血管がまばらで明るく過膨張が見られる。 | 極めて稀だがRAで予後不良なものがある。 |
| リウマチ結節 | |
| 胸膜に接する半球状ないし方形の結節、肺内の球形結節も時に見られる。 | RAで見られる。 |
| 肺出血 | |
| 局所の出血量を反映したごく淡いすりガラス影から浸潤影まで様々。 | |
| PVOD(pulmonary veno-occulusive disease)/ CH(capillary hemangiomatosis) | |
| 毛細血管通過直後の細静脈の閉塞でうっ血し毛細管周囲にあふれ肺高血圧と肺水腫をきたす。小葉中心性の淡い陰影、広範なすりガラス影や小葉間隔壁の肥厚も見られる。 | SScやMCTDに見られる。 |
RA発症後10年前後でILDを診断されるが、ついでRAとILDの同時発症が多い。10~20%はILDが先行後に関節炎を生じる。UIPとfNSIPが大部分をしめ、OPが5%。Cellular NSIPは少ない。稀ながらDADもある。
急性では肺炎の鑑別が重要で抗菌薬で改善しない陰影が移動する場合はOPを疑い気管支鏡検査を行う。広範な陰影では重症肺炎やPCPなどの感染症やDADを疑う。慢性ではHRCTでUIPパターンかNSIPパターンか判断して進行程度を長期的にみることが必要である。
UIPはステロイドや免疫抑制剤での加療は行わない。UIPであってもNSIPが混在する場合はPSL10~40mg/day、TAC、CYA、AZA、アバタセプトなどが使用されている。レフルノミドは控える。高齢、低アルブミン血症、糖尿病などではMTXも薬剤性肺障害のリスクが高い。
NSIPで浸潤影やすりガラス影が主体であればcNSIP、線維化を反映した牽引性気管支拡張が目立つようであればfNSIPと考えるが、両者の区別は困難なこともある。cNSIPはステロイド単剤で有効例が多い。fNSIPではPSL0.5mg~1mg/kg/dayで開始2~4週毎に5mgづつ漸減。免疫抑制剤はCYA 2~3mg/kg/day、TAC0.05~0.75mg/kg/day(保険適応は3mg/day)。初期から免疫抑制剤を併用する場合にはステロイドは少量にする。
OPではPSL0.5mg/kg/dayを2~4週投与後に漸減。抵抗性ではCYAやTAC、生物製剤の併用を考慮する。
DADでは早期からステロイドパルスを行う。
ILDの急性増悪ではBNP測定や心エコーで心不全を鑑別し、PCPを疑う場合はβ-Dグルカン測定や喀痰BALFのPneumocystis jirovecii のPCRを行う。MTX肺障害ではBALのCD4/CD8比の上昇や肉芽腫形成が示唆する。重症例では検査と治療を同時並行して被疑薬を中止、PCPが否定されるまでST合剤(6~12錠/day)の投与を行う。mPSLパルス療法を1週間隔で1~4コース繰り返す。他の免疫抑制剤(CYA、TAC、AZA、CYなど)も検討する。重篤になる前に挿管や人工呼吸管理を行うかの意思確認が望ましい。ネーザルハイフローなどの非侵襲的呼吸管理も試みても良い。
SScと診断されれば全例でHRCTが推奨される。ILDがあればHRCTと呼吸機能検査でlimited diseaseかextensive diseaseなのか分類する。1大動脈上部、2気管分岐部、3肺静脈合流点、4 3と5の中間、5右横隔膜上、の5スライスでおよその面積比が20%未満ならlimited、20%超ならextensive、判定不能であればFVC70%以上ならlimited、70%未満ならextensiveとする。
Extensiveで高度肺機能低下がない場合、初期導入としてCY(POCY では1~2mg/kg/dayを12ヶ月。IVCYでは500~750mgを1~3ヶ月毎に6~12回)投与後にAZAかMMFで維持療法。MMF、ニンテダニブ単独かPOCY/IVCYまたはMMFをニンテダニブに併用する(CYとMMFの同時併用は不可)。%FVC<50%、酸素療法必要な高度肺機能低下例は肺移植(60歳未満)を考慮する。POCYでは悪性腫瘍リスクが上がるため総投与量制限(36g以下)がのぞましい。高度肺機能低下例では可逆性に乏しく免疫抑制のある治療は感染リスクから死亡リスクを高める懸念があり、リスクベネフィットを考慮した治療が必要である。
LimitedであってもILD進展リスク(喫煙歴、高齢、低DLCO、6分歩行後のSpO2低下、関節炎、KL-6>1,273 U/mLなど)では治療介入を考慮する。初期導入として経口CY(IVCYでも可)投与後にAZAかMMFで維持療法。MMF、ニンテダニブ、トシリズマブ(皮下注射162mg/週)を単独か併用(CYとMMFとの同時併用は不可)。ILD進展予想低リスクでも半年~1年での病勢評価で進行確認されたら治療開始。
これらの治療に抵抗例ではレスキュー治療としてRTXの報告がある。RTXはSScの皮膚硬化に対して適応があるがILDへの適応はない。治療関連死のリスクもあるが自己末梢血幹細胞移植の有用報告もある。
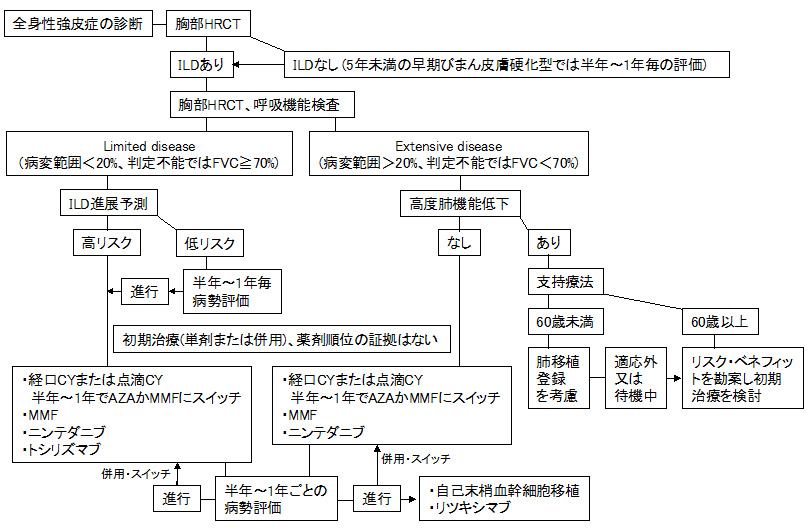
全身性強皮症に伴うILD診療フローチャート。膠原病に伴う間質性肺疾患 診断・治療指針2020より。
急速進行性で予後不良な一群があることを念頭において治療タイミングを逃さない。週単位の急性ではパルス先行と高用量PSL、免疫抑制剤単剤(CNIあるいはIVCY)、数ヶ月~年単位の進行では中~高用量PSLと早期からの免疫抑制剤、ほとんど進行しなければ経過観察のみ。
抗MDA5抗体陽性は速やかに専門施設へ転院、可能な限り感染症を除外して呼吸器症状や肺機能低下出現前での治療開始が予後を左右する。治療反応例では抗MDA5抗体110±30 unit、治療反応不良では357±208unit、また、フェリチンが活動性と相関し1600ng/ml以上では予後不良だったとの報告がある。抗MDA5抗体高力価や治療後も抗体が低下しない例は予後不良になりやすい。低酸素血症に陥ると予後は厳しい。原則mPSLパルス先行を含む高用量PSLに、CNI(TACは分2にてトラフ10ng/mL以上、またはCYAは分1にてC2で1000ng/mL以上)、IVCY(500mg/m2より開始し白血球nadirが2000~2500となるよう調整)の3剤を併用する。3剤療法に抵抗性では保険適応にないが症例報告レベルでの治療選択になる。IVCYの代わりにMMF(~3g/日。腎機能低下では減量)、RTX(1gを0週と2週の2回投与)、トファシチニブ5mg/日(CMV活性化や帯状疱疹などウイルス感染に注意が必要)、血漿交換療法(抗MDA5抗体やサイトカインの除去が効果に寄与と推測)などの有効例報告がある。トシリズマブやIVIGには筋炎に対する有効例の報告はあるがILDに対する報告はない。
抗ARS抗体陽性では病変の進行度、ILDの重症度、年齢や併存症を評価して治療選択する。抗Jo-1抗体陽性では非Jo-1抗体と比較して寛解率が高い。ステロイド単剤では減量時の再燃が多いため早期から免疫抑制剤(CY、TAC、CYA、AZAなど)の併用が推奨されている。他にRTXの有効例の報告がある。MMFやIVIGの効果は不明である。
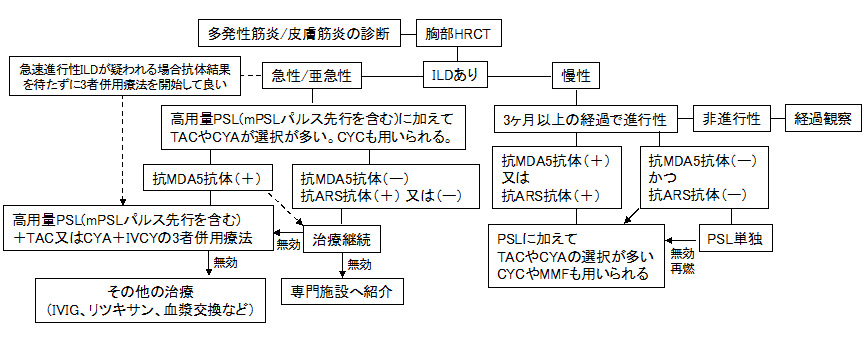
多発性筋炎/皮膚筋炎に伴うILD診療フローチャート。膠原病に伴う間質性肺疾患 診断・治療指針2020より。
NSIPやUIPが多く、LIPやOPも見られる。NSIPではステロイド(1mg/kg/日)から開始し免疫抑制剤(日本ではCYAやTACなどのCNI、欧米ではCY、AZA、MMFなどが使用されるがいずれも保険適応外)を併用することが多い。UIPでも細胞浸潤を認めることがあり治療に反応することがある。嚢胞を伴うことが多く、アスペルギスルなどの感染症合併に注意する。治療抵抗例ではRTXの報告もある。
急性ループス肺炎は稀な合併症だが予後は厳しい。免疫複合体の沈着からの組織障害が生じ、びまん性間質性リンパ球浸潤と肺胞隔壁へのIgGやC3の沈着、重症例では急性肺胞上皮障害、浮腫、硝子膜形成などびまん性肺胞障害(DAD)の所見を呈する。mPSLパルス後の高用量ステロイドにIVCY、あるいはMMF、CNI、AZAなどの免疫抑制剤併用。RTX、血漿交換、IVIGなどの報告例がある。
慢性ILDではHRCTですりガラス影を認め炎症が比較的高度な場合はステロイドによる治療が行われ、反応性が乏しい場合はCY、MMF、AZA、RTXなどの使用報告がある。
SScと異なり治療反応性が良い。急性ではステロイド高用量、治療抵抗性では免疫抑制剤併用、慢性で活動性がある場合はSScに類似しCYが選択される。日本人MCTDの7%に合併する肺高血圧症は最も重要な予後不良因子である。ステロイドと免疫抑制剤(CY)の併用を行うがSScに合併した場合より反応性が見られる。
XPでは両側下肺野優位に網状影や輪状陰影を認めることが多く、CTでは胸膜直下の網状影やすりガラス影、蜂巣肺、牽引性気管支拡張などが見られる。MPA-ILDの61%がUIPかpossible UIPで、軽微な浸潤影や気管支壁肥厚、嚢胞、すりガラス影なども見られることがある。
ANCA血管炎診療ガイドラインに従って治療する。寛解導入はステロイド単独より、ステロイド+静注CY(経口CYを用いても良いが、経口より静注が優先される。RTXが適切と判断される場合はCYの代替として用いても良い)。CY、RTXともに使用できない場合はステロイド+MMFが考慮される。重症な腎障害や肺胞出血を伴うAAVでは血漿交換を併用することがある。寛解維持ではステロイドに加えAZAを併用する。他の併用薬剤として、RTX、MTX、MMFが選択肢となりうる。
ニンテダニブ(オフェブ150mg2回/日で投与)はチロシンキナーゼ阻害剤で、VEGF受容体、PDGF受容体、FGF受容体など受容体型やSrc、Lckなど非受容体型のチロシンキナーゼの活性に重要なATP結合サイトを占拠する。難治性病態である線維化の進行を遅らせる効果があるが、副作用も多く注意が必要である。
創傷治癒遅延や消化管穿孔、血栓塞栓症など重篤な副作用があり、外科処置、気胸、胃潰瘍、心筋梗塞などの既往がある場合、早めに異常の発見に努める。中等度以上の肝障害では使用しない。妊婦は禁忌。
頻度の高い副作用では肝障害、下痢、悪心・嘔吐が多い。
AST、ALTが基準値上限の3倍を超えた場合は減量や中断し、100mg2回/日で再開。症状あれば投与中止。
下痢は止瀉剤(ロペミンなど)や整腸剤、補液を投与、効果不十分では中断し、100mg2回/日で再開。高度であれば投与中止。
悪心や嘔吐はドパミン受容体拮抗剤(プリンペランやナウゼリンなどの)投与、効果不十分では中断し、100mg2回/日で再開。高度であれば投与中止。
日本ベーリンガーインゲルハイム株式会社「オフェブ適正使用ガイド」より