大阪大学大学院医学系研究科
呼吸器・免疫内科学
Department of Respiratory Medicine and Clinical Immunology, Graduate School of Medicine, The University of Osaka
1951年に、Jacob ChurgとLotte Straussによって提唱された疾患で、気管支喘息やアレルギー性鼻炎が先行し、好酸球増多を伴った壊死性肉芽腫性血管炎である。2012年、Chapel Hill会議では、主に小血管に病変がある疾患として好酸球性多発血管炎性肉芽腫症(Eosinophilic Granulomatosis with Polyangiitis: EGPA)の名称が提案された。従来は、臨床所見と組織所見があればアレルギー性肉芽腫性血管炎(Allergic Granulomatous Angitis:AGA)と呼び、臨床所見のみであればChurg-Strauss症候群(CSS)と呼んでいた。
病態は末梢血好酸球増多と浸潤による好酸球性炎症、ANCA関連血管炎としての微小血管障害、血管内外での肉芽腫形成性炎症の特徴を混合する。EGPAのゲノム解析ではpANCA陽性EGPAはHLA-DQとの関連が断然強く、pANCA陰性EGPAはTSLP、C5ORF6、GPA33などの免疫分子との関連が強い(Lyons et al. Nat Commun 10:5120 2019)。
気管支喘息やアレルギー性鼻炎が先行する。その後、末梢好酸球の増加とともに、発熱などの全身症状や各種の全身症状が現れる。多発単神経炎により下肢あるいは上肢の知覚障害(しびれや痛み)や運動障害(これらはしばしば治療後も残る)、鼻茸を伴う好酸球性副鼻腔炎や、好酸球浸潤を伴う皮膚、肺、消化管、心筋などの炎症もしばしば見られる。血管炎による、中枢神経障害(脳梗塞症状)、消化管穿孔、心血管系障害、肺胞出血、腎障害などを起こすと重症化することがある。EGPAで見られる症状はANCAの有無で頻度が異なり、ANCA陽性では耳鼻咽喉症状、神経症状、腎障害が、ANCA陰性では心血管系症状が比較的頻度が高い。呼吸器症状、腎障害、消化器症状に関してはANCA有無で差はない。死亡率と関連する5つの予後不良因子(Five Factor Score。65歳以上、Cr1.7mg/dL以上の腎不全、心不全症状、重症消化管病変、耳鼻咽喉症状がない)がある。
本邦でのEGPA188名の臓器障害の頻度(Saku A et al.J Rheumatol 45:1159-1166.2018)
| 症状 | 頻度 | 症状、徴候 |
|---|---|---|
| 神経症状 | 88% | 多発単神経炎(下肢を中心とした四肢の痺れや痛みによる感覚障害、筋力低下による運動機能障害)など |
| 耳鼻咽喉症状 | 50% | 好酸球性副鼻腔炎、鼻茸、鼻粘膜炎、味覚障害、中耳炎など |
| 皮膚症状 | 41% | 紫斑、網状皮斑、皮下出血、結節性紅斑など |
| 呼吸器症状 | 34% | 好酸球性肺炎、間質性肺炎、浸潤影・結節影、肺胞出血、胸膜炎など |
| 腎障害 | 18% | 蛋白尿、糸球体腎炎など |
| 消化器症状 | 12% | 腹痛、下痢、消化管出血、消化管穿孔など |
| 心血管系症状 | 11% | 不整脈、冠動脈炎、狭心症、心不全、心外膜炎など |
| 眼症状 | 5% | 強膜炎、眼窩炎症、偽腫瘍、虚血性視神経症など |
他に、全身症状(発熱、倦怠感、体重減少など)、関節・筋症状(関節痛や筋肉痛など)もよく見られる。中枢神経症状(脳梗塞、脳出血、脳血管炎など)では後遺症を残す。
血液検査では、炎症所見(CRP上昇、血沈亢進)、好酸球増加、血清IgE高値、MPO-ANC上昇がみられる。MPO-ANCAは、本症の40-70%程度で陽性となる。肺病変を伴う場合の肺胞洗浄液に好酸球増加が見られることがある。組織検査では、肺病変、神経病変、皮膚病変などの病変部位に、好酸球浸潤や肉芽腫の形成をみとめる。
| 主要臨床所見 | ||
|---|---|---|
| 1. | 気管支喘息あるいはアレルギー性鼻炎 | |
| 2. | 好酸球増加(末梢血白血球の10%以上、または1500/μL以上) | |
| 3. | 血管炎症状:発熱(38℃以上、2週間以上)、体重減少(6ヶ月以内に6kg以上)、多発性単神経炎、消化管出血、紫斑、多関節痛(炎)、筋肉痛(筋力低下)、紫斑のいずれか1つ以上 | |
| 臨床経過の特徴 | ||
| 気管支喘息、アレルギー性鼻炎、好酸球増加が先行し、血管炎による症状が出現する | ||
| 主要組織所見 | ||
| 1. | 周囲組織に著明な好酸球浸潤を伴う細小血管の肉芽腫またはフィブリノイド壊死性血管炎の存在 | |
| 2. | 血管外肉芽腫の存在 | |
| 血管炎類似疾患を除外し、小~中型血管炎の診断がなされた上で点数計算を行い、7項目計6点以上でEGPAと分類する | |
| 臨床 | 1. 閉塞性気道病変(+3) |
| 2. 鼻茸(+3) | |
| 3. 多発性単神経炎(+1) | |
| 検査 | 1. 血中好酸球≧1000/μL(+5) |
| 2. 生検:血管外の好酸球主体の炎症(+2) | |
| 3. cANCA or PR3-ANCA陽性(-3) | |
| 4. 血尿(-1) | |
| 好酸球増多症候群 | 末梢血好酸球増加(>1500/μl)が6ヶ月以上、寄生虫・アレルギーなどの疾患が除外され、好酸球浸潤による臓器障害(心、肺、中枢神経系、皮膚)を伴う。EGPAはアレルギー背景の血管炎。 |
| 好酸球性肺炎 | 好酸球肺浸潤、末梢血好酸球増加(>6%、又は>400/μl)、咳、喀痰、呼吸困難、発熱を呈する。喫煙との関連の報告もある。 |
| アスピリン喘息 | COX1阻害作用のNSAIDsによる非アレルギー性喘息で、鼻茸を伴う好酸球性副鼻腔炎の合併が多い。 |
| アレルギー性気管支肺真菌症 | ABPMは末梢血好酸球数増多、血清IgE高値を示す。血清アスペルギルス抗原特異的IgEや各種沈降抗体が診断に有用。 |
| IgG4関連疾患 | 血清IgG4高値(135mg/dl以上)、腫瘤病変部でIgG4産生形質細胞を認める。4割にアレルギー症状が見られる。 |
| 結節性多発動脈炎 | 中型の動脈壁の炎症。血管炎による梗塞で多彩な臓器症状を呈する。 |
| 顕微鏡的多発血管炎 | 末梢神経、腎臓、肺、皮膚などの壊死性小血管炎。末梢神経障害、壊死性糸球体腎炎、肺毛細血管炎など伴う。pANCAが多い。 |
| 多発血管炎性肉芽腫症 | 耳や鼻など上気道、肺、腎臓の壊死性肉芽腫性血管炎。cANCAが多い。 |
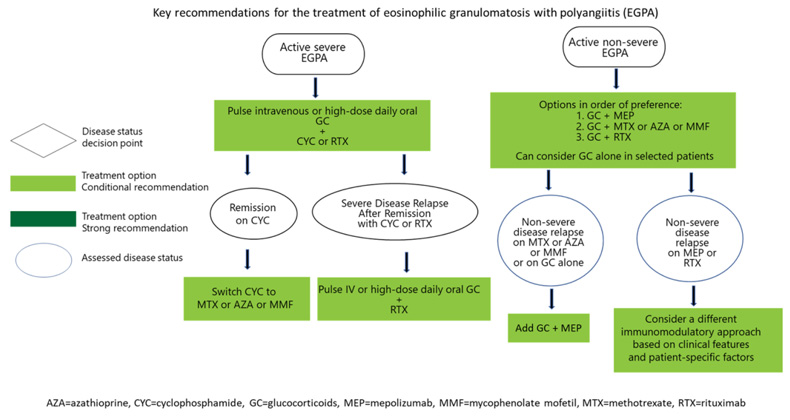
寛解導入療法は、臓器・生命を脅かす新規発症や再発EGPAではステロイドパルスや高容量ステロイドにシクロホスファミドやRTXを追加する、臓器・生命を脅かさない新規発症や再発EGPAでは経口ステロイド、難治性では抗IL-5抗体メポリズマブ(ヌーカラ300mgを4週毎皮下注)や抗IL-5受容体抗体ベンラリズマブ(ファセンラ30mgを4週毎皮下注)を併用する。
寛解維持療法では臓器・生命を脅かすEGPAではMTX、AZA、IL-5阻害薬、RTXのいずれか、臓器・生命を脅かさないEGPAではIL-5阻害薬を使用。
シクロホスファミド投与量は年齢、腎機能、白血球数、好中球数に応じて適宜減量する。治療抵抗性の神経障害が残る場合は高用量ガンマグロブリン点滴療法(献血ベニロン400mg/kgを5日間点滴)が保険適応ではある。疾患活動性が落ち着いた後も末梢神経障害は長期に残存することが多い。
メポリズマブとベンラリズマブはともに有効だが、ステロイド減量効果はベンラリズマブがよかったという報告がある。ステロイド減量のためのアバコパンは本邦から黄疸を伴う重篤な肝障害の報告が目立つ。
疾患活動性にBVAS(Birmingham Vasculitis Activity Score)、重症度判定にEUVAS(European Vasculitis Study)が用いられることがある。
| 寛解導入療法 | |
|---|---|
| 重症で活動性あり | 初期治療として点滴パルスまたは高用量経口GCのいずれか |
| CYまたはRTXのいずれか | |
| MEPOより、CYまたはRTX | |
| 非重症で活動性あり | MTX、AZA、MMFとGCの併用より、MEPOとGCの併用 |
| GC単独より、MTX、AZA、MMFとGCの併用 | |
| CYやRTXとGCの併用より、MTX、AZA、MMFと GCの併用 | |
| 寛解維持療法 | |
| CYで寛解した重症EGPAは、維持にRTXよりMTX、AZA、MMF | |
| 寛解状態にある重症EGPAは、維持にMEPOよりMTX、AZA、MMF | |
| EGPAのGC療法の期間は、患者の臨床状態、価値観、希望に基づく | |
| 再発の治療 | |
| CYで寛解導入後、重篤な疾患症状で再発したEGPAは、再寛解導入にCYよりRTX | |
| RTXによる寛解導入後、重篤な疾患症状を伴って再発したEGPAは、再寛解導入にCYに切り替えるよりRTX | |
| MTX、AZA、MMFを服用中、非重症の症状(喘息、副鼻腔疾患)で再発したEGPAは、他の薬剤に切り替えるよりMEPOを追加 | |
| 低用量GCで、他の治療を受けていないにもかかわらず、非重篤な疾患症状(喘息、副鼻腔疾患)で再発したEGPAは、MTX、AZA、MMFより、MEPOを追加する | |
| MTX、AZA、MMFを服用中、非重症の症状(喘息、副鼻腔疾患)で再発したEGPAおよび高血清IgEの患者は、オマリズマブよりもMEPOを追加する | |
| その他の考慮 | |
| 新たにEGPA診断されたロイコトリエン阻害薬内服患者は、ロイコトリエン阻害薬の中止よりも継続 | |
| ロイコトリエン阻害薬は、活動性喘息、副鼻腔疾患を伴うEGPAに禁忌ではない | |
| EGPAは、診断時に心エコー検査を受ける | |
| EGPAは、治療指針として5因子スコアを使用する | |
| EGPAの副鼻腔病変に鼻洗浄や局所療法(抗生物質、潤滑剤、GC)が検討されることがある。 | |
| CYやRTXを投与されているEGPAに、PCP肺炎予防のため予防薬を処方する | |
GC(グルコココルチコイド)、CY(シクロホスファミド)、RTX(リツキシマブ)、MTX(メトトレキサート)、AZA(アザチオプリン)、MMF(ミコフェノール酸モフェチル)、MEPO(メポリズマブ)。本邦ではIL-5阻害薬として、メポリズマブとベンラリズマブの使用が可能である。
| 小~中血管炎の生命予後を予測するFive Factor Score | |
|---|---|
| 1. | 65歳以上 |
| 2. | 腎不全(安定したピーク値で1.7mg/dL以上) |
| 3. | 心不全(肺水腫などの臨床症状の存在のみに基づいて判断。BNP値や心エコー所見は考慮しない) |
| 4. | 重度消化管障害(腸穿孔、出血、膵炎のみを対象とし、虫垂炎や胆嚢炎は含めない) |
| 5. | ENT(耳鼻咽喉)症状がない(耳鼻咽喉科専門医による診察とCT画像で確認された臨床症状) |
全身性壊死性血管炎である、結節性多発動脈炎、顕微鏡的多発血管炎、多発血管炎性肉芽腫症、好酸球性多発血管炎性肉芽腫症、の4疾患での5年死亡率はスコアが0で9%、1で21%、2以上で40%となる。スコアは活動性血管炎に直接起因するものをとる。
65歳以上の高齢者ではGCと細胞傷害性薬は感染症の発生リスクに繋がる。累積投薬量を少なくしたり、寛解導入療法から早期に副作用の少ない維持療法に切り替えると感染症の発生は低くなる。
肺胞出血は死亡リスクを8.6倍に上げるが、重度の肺胞出血は重度の腎不全患者のごく一部で、腎不全でリスク因子としてカウントされる。単に血痰だけでは転帰に影響ない。
ENT症状はGPAとEGPAのみで使用し、ENT症状があると予後良好と関連する。
FFSは、臨床医が全身性壊死性血管炎の予後を予測するために使用する単純なスコアの一つだが、治療選択を行うためのツールとして検証される必要がある。